Neues aus der Praxis: Apixaban oder Rivaroxaban zur initialen und weiteren Behandlung eines Patienten mit Magenkarzinom und Lungenembolie?
Ein junger Patient mit aktivem Magenkarzinom soll aufgrund einer Lungenembolie (LE) antikoaguliert werden. Eine mögliche Therapieoption stellt dabei die Behandlung mit einem NOAC dar. Doch das Blutungsrisiko des Patienten ist durch den gastrointestinalen (GI-)Tumor erhöht.
Anhand eines fiktiven Patientenfalls möchten wir in dieser Artikelreihe auf eine besondere Situation in der klinischen Praxis eingehen und die Herangehensweise sowie mögliche leitliniengerechte Lösungen aufzeigen. Halten Sie in den nächsten Monaten Ausschau nach neuen Fällen!
Heute: „Der junge Mann mit aktivem Magenkarzinom und LE“
Anamnese
Bei einem jungen Patienten (32 Jahre) mit aktivem Magenkarzinom wird bei einer Kontrolluntersuchung eine asymptomatische, inzidentelle Lungenembolie (LE) festgestellt. Da der Patient zum Diagnosezeitpunkt hämodynamisch stabil ist, soll die initiale Antikoagulation mit einem Nicht-Vitamin-K-abhängigen oralen Antikoagulans (NOAC) unverzüglich begonnen werden. Doch GI-Tumore gehören zu den Tumorentitäten mit hohem GI-Blutungsrisiko.1 Welches NOAC ist zur initialen und weiteren Behandlung von venösen Thromboembolien (VTE) bei Patient:innen mit GI-Tumoren geeignet? Nachfolgend werfen wir einen Blick auf Apixaban (ELIQUIS®) und Rivaroxaban (Xarelto®), die am häufigsten verordneten NOACs.2
Klinische Evidenz von Apixaban und Rivaroxaban
Bei Patient:innen mit krebsassoziierter Thrombose und einer luminalen GI-Malignität deutete sich unter einer Rivaroxaban-Behandlung ein höheres Risiko für schwere GI-Blutungen als unter niedermolekularen Heparinen (NMH) an (Select-D-Studie3, 4, ††; Abb. 1).
Hingegen zeigte sich in der CARAVAGGIO-Studie5, dass Apixaban bei der Behandlung von krebsassoziierter VTE eine mit Dalteparin vergleichbare Option darstellen kann – nicht nur bezüglich der Verhinderung von VTE-Rezidiven. Auch das Risiko für schwere Blutungen, inklusive GI-Blutungen, war unter Apixaban vergleichbar mit Dalteparin.5 Obwohl bei ungefähr einem Drittel der Studienteilnehmer:innen eine Tumorerkrankung mit GI-Lokalisation vorlag, wurde kein Signal für erhöhte Raten von GI-Blutungen beobachtet.5 Dementsprechend hat die CHEST-Guideline 2021 Apixaban neben NMH als bevorzugte Option zur Behandlung von Patient:innen mit luminalen GI-Tumoren deklariert.6
Nähere Informationen zu den klinischen Studien CARAVAGGIO5 und SELECT-D3 entnehmen Sie bitte folgendem Akkordeon.
In den Studien CARAVAGGIO5 und SELECT-D3 überzeugten sowohl Apixaban als auch Rivaroxaban als mögliche alternative Behandlungsoptionen von Patient:innen mit krebsassoziierter VTE vs. Dalteparin.*
Apixaban
In der CARAVAGGIO-Studie4
(1.170 Proband:innen) traten unter Apixaban im Vergleich zu Dalteparin
-
nummerisch weniger VTE-Rezidive (primärer Endpunkt; HR#: 0,63; 95 %-KI: 0,37-1,07) und eine
-
vergleichbare Rate für schwere Blutungen** (HR: 0,82; 95 %-KI 0,40-1,69) auf.
Rivaroxaban
In der SELECT-D-Studie3
(406 Proband:innen) traten unter Rivaroxaban im Vergleich zu Dalteparin
-
weniger VTE-Rezidive (primärer Endpunkt; HR: 0,43; 95 %-KI: 0,19-0,99) und eine
-
vergleichbare Rate für schwere Blutungen†† (HR: 1,83; 95 %-KI: 0,68-4,96) auf.
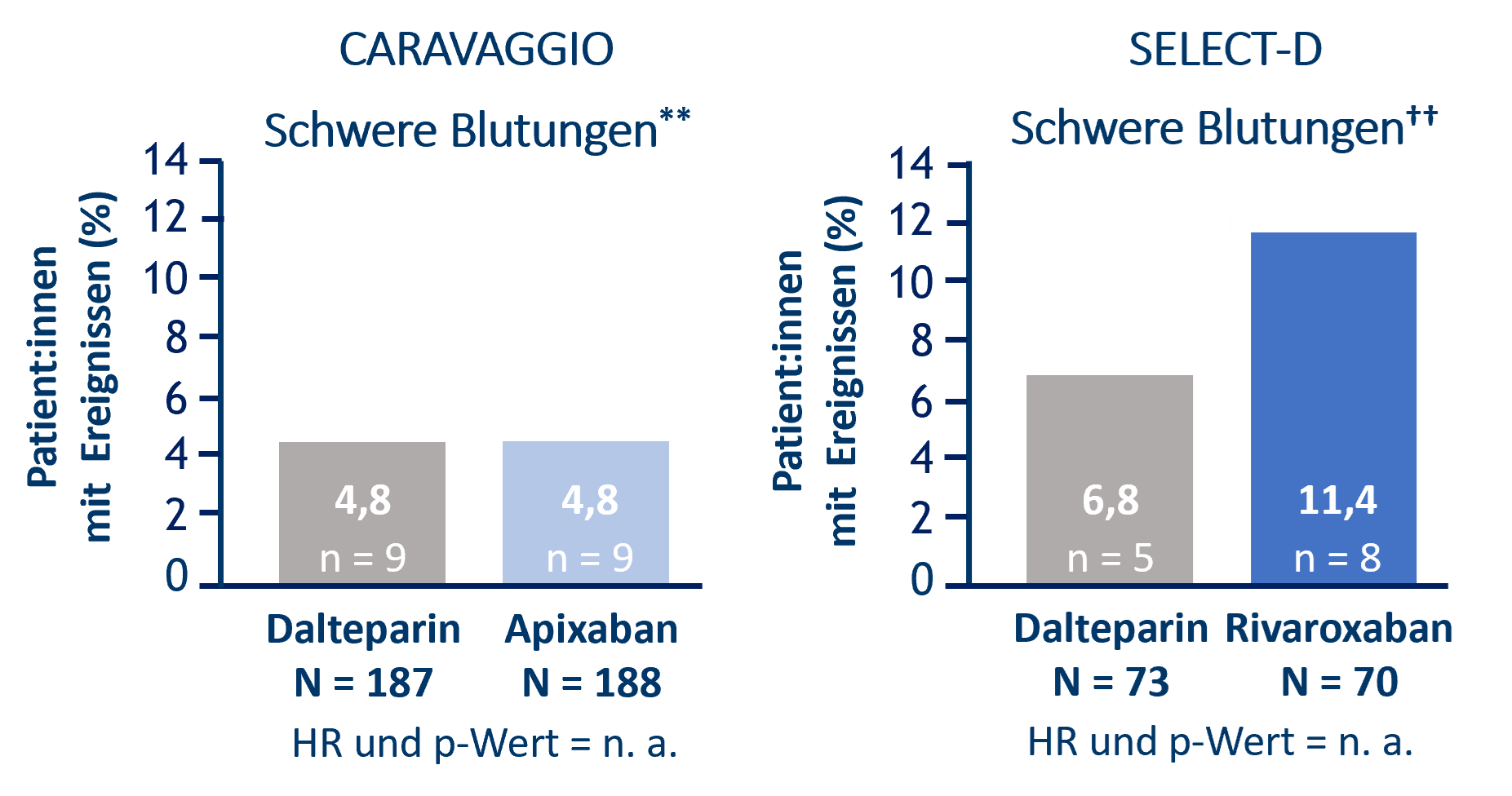
Abb. 1: Klinische Evidenz zur VTE bei Patient:innen mit GI-Tumoren: Kumulative Ereignisraten (in %) für schwere Blutungen unter Apixaban versus Dalteparin (CARAVAGGIO7) bzw. Rivaroxaban versus Dalteparin (SELECT-D4). n. a. = ohne Angabe. Modifiziert nach Ageno et al.7 und Voigtländer et al.4 Es existieren keine prospektiven NOAC-Vergleichsstudien, daher können keine direkten Vergleiche zwischen den Präparaten gezogen werden.
Apixaban und Rivaroxaban im Versorgungsalltag: Gibt es Unterschiede?
In der unabhängigen, retrospektiven Kohorten-Studie von Dawwas et al. aus 2022 (basierend auf US-amerikanischen Versicherungsdaten von 2015 bis 2020) wurde Apixaban und Rivaroxaban (n jeweils = 18.618 mit Neuverschreibung des jeweiligen NOACs) in den ersten 6 Monaten analysiert.†,* Nach Propensity Score Matching war Apixaban mit einer niedrigeren Rate für VTE-Rezidive (Hazard Ratio (HR): 0,77; 95 %-KI 0,69-0,87) und Blutungen (HR: 0,60; 95 %-KI 0,53-0,69) gegenüber Rivaroxaban assoziiert. Die Behandlung mit Apixaban war mit einer geringeren Rate für GI-Blutungen (HR: 0,60; 95 %-KI 0,53-0,69) sowie für intrakranielle Blutungen (HR: 0,54; 95 %-KI 0,14-1,20) gegenüber Rivaroxaban assoziiert.
Näheres zum Studiendesign der retrospektiven Datenanalyse von Dawwas et al.8 entnehmen Sie bitte nachfolgendem Akkordeon.
- Zeitraum: 01.01.2015-30.06.2020
- Datenquelle: Optum Insight Clinformatics Database, eine kommerzielle US-Versicherungsdatenbank
- 49.900‡ Erwachsene TVT/LE-Patient:innen mit Apixaban-/Rivaroxaban-Neuverordnung innerhalb von 30 Tagen nach der Diagnose
- Propensity-Score-Analyse mit Hilfe des Regressionsmodells PROC LOGISTIC; SAS Institut
- Follow-up ab der 1. Verschreibung bis zum Auftreten eines Endpunkts, Absetzen oder Wechsel der Indexmedikation, Ausscheiden aus dem Gesundheitsplan für mehr als 30 Tage oder Ende des Studienzeitraums
- Medianes Follow-up: 102 Tage für Apixaban und 105 Tage für Rivaroxaban
- Primärer Effektivitätsendpunkt: VTE-Rezidive∆
- Primärer Verträglichkeitsendpunkt: Schwere GI- oder intrakranielle Blutungen∆
Eine Subgruppenanalyse‡ dieser US-Versorgungsdaten betrachtete Patient:innen mit bzw. ohne Krebserkrankung und kam zu folgenden Ergebnissen (Abb. 2):
Bei Patient:innen mit Krebserkrankung (jeweils n = 4.096) ist Apixaban im Versorgungsalltag mit
- einer vergleichbaren Rate an VTE-Rezidiven∆ (HR: 0,96; 95 %-KI 0,76 – 1,23) und
- weniger schweren GI- oder intrakraniellen Blutungen∆ (HR: 0,71; 95 %-KI 0,56 – 0,89) gegenüber Rivaroxaban assoziiert.†
Bei Patient:innen ohne Krebserkrankung (jeweils n = 14.396) ist Apixaban im Versorgungsalltag mit
- einer geringeren Rate an VTE-Rezidiven∆ (HR: 0,71; 95 %-KI 0,61 – 0,81) und
- weniger schweren GI- oder intrakraniellen Blutungen∆ (HR: 0,60; 95 %-KI 0,51 – 0,70) gegenüber Rivaroxaban assoziiert.†
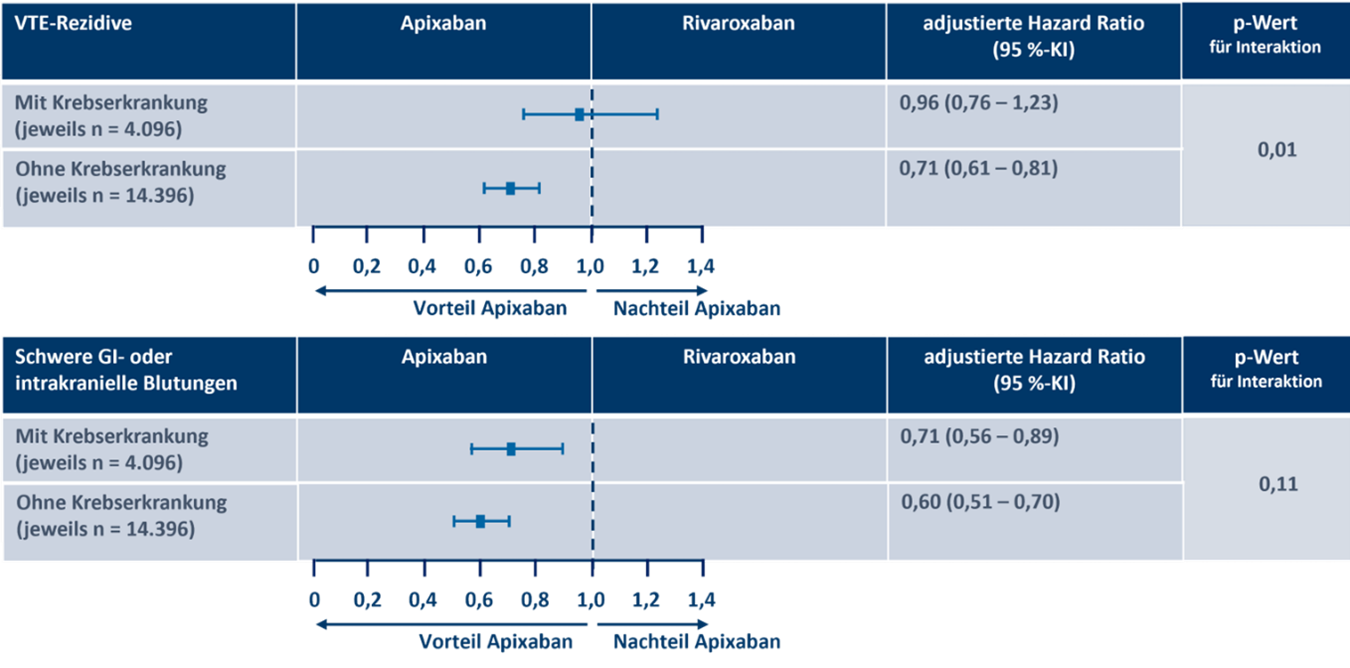
Abb. 2: Subgruppenanalyse‡ der Versorgungsdaten: VTE-Rezidive∆ sowie schwere GI- und klinisch relevante nicht schwere (CRNM) Blutungen∆ unter Apixaban bzw. Rivaroxaban bei VTE-Patient:innen mit oder ohne Krebserkrankung. Modifiziert nach Dawwas et al.8,† Es existieren keine prospektiven NOAC-Vergleichsstudien, daher können keine direkten Vergleiche zwischen den Präparaten gezogen werden.
Fazit
Die CARAVAGGIO-Studie zeigte eine vergleichbare Wirksamkeit und Sicherheit von Apixaban gegenüber NMH in der VTE-Behandlung bei Patient:innen mit aktiven GI-Tumoren.5 Weiterhin hat die CHEST-Guideline 2021 Apixaban neben NMH als bevorzugte Option zur VTE-Behandlung von Patient:innen mit luminalen GI-Tumoren deklariert.6 Die Versorgungsdaten von Dawwas et al. ergänzen die Ergebnisse der klinischen Studien von CARAVAGGIO und SELECT-D.3, 5, 8 Darüber hinaus assoziierte Apixaban im Vergleich zu Rivaroxaban bei Patient:innen mit krebsassoziierter VTE in den ersten sechs Monaten der Antikoagulationstherapie mit einer vergleichbaren Effektivität und einem geringeren Risiko für schwere GI- und intrakranielle Blutungen.8,‡,* Demzufolge kann Apixaban, unter sorgfältiger Abwägung§ des Nutzens gegenüber dem Blutungsrisiko‡‡, eine gute Behandlungsoption für unseren LE-Patienten mit Magenkarzinom innerhalb der Therapiephase darstellen. Unser Patient erhält daher in diesem fiktiven Bespiel zur VTE-Behandlung initial Apixaban 10 mg 2 x tägl. für 7 Tage, anschließend wird die Dosis auf 5 mg 2 x tägl. angepasst.9
VTE: venöse Thromboembolie (tiefe Venenthrombose (TVT) und/oder Lungenembolie (LE))
CRNM = clinically relevant nonmajor
†† Patient:innen, die bei Randomisierung einen Tumor im Bereich der Speiseröhre bzw. des gastroösophagealen Übergangs (n = 30), des Magens (n = 11) oder des Dickdarms/Rektums (n = 102) hatten. Nach Review der ersten 220 Patient:innen durch das „Data and Safety Monitoring Committee“ ergab sich ein nicht-signifikanter Unterschied der schweren Blutungen zwischen Rivaroxaban und Dalteparin bei 19 Patient:innen mit Krebserkrankung des Ösophagus oder im gastroösophagealen Übergang. Patient:innen mit diesen Krebserkrankungen wurden daraufhin nicht mehr in die Studie eingeschlossen.
* Es existieren keine prospektiven NOAC-Vergleichsstudien, daher können keine direkten Vergleiche zwischen den Präparaten gezogen werden.
# p < 0,001 für Nicht-Unterlegenheit; 0,09 für Überlegenheit.
** Bei Patient:innen mit kolorektalem Karzinom, Pankreaskarzinom, hepatobiliären Tumoren sowie Tumoren im oberen GI-Trakt.
† Limitationen: • Beobachtungsstudien zeigen nur Assoziationen zwischen Variablen, keine Kausalität. • Laborparameter waren nur für eine kleine Gruppe der Patient:innen vorhanden. Diese wiesen aber eine gut ausbalancierte Verteilung der Baseline-Labormessungen auf, inklusive Kreatinin, Cholesterin, Triglyzeride und Hämoglobin A1c. • Wie bei jeder Versicherungsdatenbank besteht die Möglichkeit von Kodierungsfehlern und fehlenden Daten. • Eine Adjustierung / Ein Matching ist nur für die bekannten demografischen und klinischen Patient:innencharakteristika möglich; für potenzielle nicht beobachtbare Störgrößen kann nicht adjustiert werden. • Die Kohorte war auf privat versicherte VTE-Patient:innen beschränkt. Dies könnte die Generalisierbarkeit auf andere Populationen einschränken. • Nur schwere Ereignisse, die zur Hospitalisierung führten, gingen in die Auswertung ein. • Der Vergleich der NOACs ermöglicht nur die Generierung von Hypothesen. Diese Ergebnisse müssen von randomisierten, kontrollierten Interventionsstudien bestätigt werden.
‡ In der Subgruppenanalyse waren in beiden NOAC-Gruppen jeweils 4.069 Patient:innen mit Krebs und 14.396 Patient:innen ohne Krebs eingeschlossen.
∆ VTE-Rezidive sowie schwere intrakranielle und gastrointestinale Blutungen wurden anhand der zuerst gelisteten ICD-9-CM und ICD-10-CM Codes bei Krankenhausentlassung definiert.
§ Patient:innen mit aktiver Krebserkrankung können ein hohes Risiko sowohl für venöse Thromboembolien als auch für Blutungen haben. Wenn Apixaban zur Behandlung von TVT oder LE bei Krebspatient:innen in Erwägung gezogen wird, sollte eine sorgfältige Abwägung des Nutzens gegen das Risiko erfolgen.
‡‡ Apixaban ist kontraindiziert bei malignen Neoplasien mit hohem Blutungsrisiko.9
- Riess H, Angelillo-Scherrer A, Alt-Epping B, Langer F, Wörmann B, Pabinger-Fasching I. Onkopedia Leitlinien - Thromboembolien bei Tumorpatienten (früher: Venöse Thromboembolien (VTE) bei Tumorpatienten); 2020 [eingesehen am 12.12.23]. Available from: URL: https://www.onkopedia.com/de/onkopedia/guidelines/thromboembolien-bei-tumorpatienten-frueher-venoese-thromboembolien-vte-bei-tumorpatienten/@@guideline/html/index.html.
- Arzneimittel-Atlas 2022 [eingesehen am 12.12.23]. Available from: URL: https://www.arzneimittel-atlas.de/arzneimittel/b01-antithrombotische-mittel/verbrauch/.
- Young AM et al. Comparison of an Oral Factor Xa Inhibitor With Low Molecular Weight Heparin in Patients With Cancer With Venous Thromboembolism: Results of a Randomized Trial (SELECT-D). J Clin Oncol 2018; 36(20):2017–23.
- Voigtlaender M et al. Neue Studiendaten zur Therapie der tumorassoziierten venösen Thromboembolie mit DOAKs. Phlebologie 2018; 47(06):309–17.
- Agnelli G et al. Apixaban for the Treatment of Venous Thromboembolism Associated with Cancer. N Engl J Med 2020; Apr 23;382(17):1599-1607.
- Stevens SM et al. Antithrombotic Therapy for VTE Disease: Second Update of the CHEST Guideline and Expert Panel Report - Executive Summary. Chest 2021; 160(6):2247–59.
- Ageno W et al. Bleeding with Apixaban and Dalteparin in Patients with Cancer-Associated Venous Thromboembolism: Results from the Caravaggio Study. Thromb Haemost 2021; 121(05):616–24 [eingesehen am 1/13/2021].
- Dawwas GK et al. Risk for Recurrent Venous Thromboembolism and Bleeding With Apixaban Compared With Rivaroxaban: An Analysis of Real-World Data. Ann Intern Med 2022; 175(1):20–8.
- Fachinformationen Eliquis® 5 mg, 2,5 mg, aktueller Stand.

