csDMARD: konventionelles synthetisches krankheitsmodifizierendes Antirheumatikum
IL17-A: Interleukin 17-A
IL17-Ai: Interleukin 17-A-Inhibitor
TNFi: Tumornekrosefaktor-Inhibitor
ACR50: American College of Rheumatology, 50 % Ansprechen;
PASI 100: 100%ige Verbesserung der PASI-(Psoriasis Area Severity Index) Kriterien im Vergleich zum Ausgangswert
Taltz<sup>®</sup> versus Adalimumab bei PsA: Welchen Vorteil kann Taltz<sup>®</sup> bieten?
Viele PsA<sup>+</sup>-Patient:innen sind nicht nur durch Gelenkschmerzen, sondern auch durch die Hautsymptomatik deutlich eingeschränkt. Für eine umfassende Therapie sollten beide Aspekte adressiert werden. Taltz<sup>®1</sup> konnte eine bessere Wirksamkeit auf die Haut als Adalimumab zeigen<sup>2</sup> – bei gleicher Wirksamkeit auf die Gelenke.<sup>3</sup>
Heterogenes Krankheitsbild der PsA
Eine Psoriasis-Arthritis+ (PsA) kann sich bei jedem Betroffenen anders manifestieren: Die Ausprägung der 6 möglichen Krankheitsdomänen periphere Arthritis, Hautbeteiligung, Nagelbeteiligung, axiale Beteiligung, Daktylitis und Enthesitis kann sehr unterschiedlich ausfallen. Die Group for Research and Assessment of Psoriasis and Psoriasis Arthritis (GRAPPA) gibt in ihrer Guideline4 folgende allgemeine Empfehlungen zur Therapie von PsA:
- Wichtigste Therapieziele:
- Erreichen der geringstmöglichen Krankheitsaktivität bei allen Domänen. Je nach Definition ist dies eine Remission oder eine geringe oder minimale Krankheitsaktivität.
- Optimierung des funktionellen Status und der Lebensqualität sowie bestmögliches Vermeiden von strukturellen Schäden
- Jede einzelne betroffene Domäne sollte therapiert werden.
- Die gängigen Diagnosekriterien sollten angewendet werden.
- Komorbiditäten und deren Einfluss auf die Therapie sollten berücksichtigt werden.
- Therapieentscheidungen werden von Behandelndem und Patient:in gemeinsam getroffen (Shared Decision Making).
- Regelmäßige Kontrollen mit geeigneter Evaluation und ggf. Anpassungen der Therapie werden empfohlen.
Für die periphere Arthritis werden bei unzureichender csDMARD-Wirkung vor allem TNFα-Inhibitoren sowie alle verfügbaren Interleukin-Inhibitoren (ausgenommen IL-6-Hemmer) empfohlen. Ist eine Hautsymptomatik vorhanden, zeigen laut GRAPPA fast alle DMARDs eine gute Wirksamkeit, bei Nagelpsoriasis wirken TNFα-Inhibitoren, IL-Inhibitoren sowie PDE-4-Hemmer am besten.4
Ein Leiden kommt selten allein
In der Praxis treten bei einer PsA die Krankheitsdomänen periphere Arthritis mit den dafür typischen Gelenksymptomen und eine Hautbeteiligung häufig zusammen auf. Diese Kombination belastet viele Betroffene doppelt: Wer an chronischen Gelenkschmerzen leidet, kann ggf. den Alltag nicht mehr wie gewohnt bestreiten und zieht sich immer mehr zurück. Im Zusammenspiel mit einer kutanen Manifestation und der damit verbundenen Angst vor einer Stigmatisierung kann die PsA deshalb auch eine psychische Belastung sein. Somit liegt es auf der Hand, dass sich Betroffene eine Therapie wünschen, die diese beiden Domänen gut adressiert.
Mit Taltz® Gelenke und Haut kombiniert behandeln
Die eingangs erwähnte Guideline empfiehlt bei Gelenk- und Hautmanifestationen als first-line Biologikum TNF- oder IL-17-Inhibitoren. Behandelnde haben somit die Wahl zwischen den beiden Wirkstoffklassen. Head-to-Head-Studien können in diesem Szenario eine Antwort auf die Frage geben, welcher Wirkansatz voraussichtlich das beste Therapieergebnis erzielt.
Welche ist besser für den jeweiligen Patienten geeignet? Eine Antwort können Head-to-Head-Vergleiche liefern.
Der IL-17A-Inhibitor Taltz® (Ixekizumab) ist bisher der einzige IL-17Ai, der eine Überlegenheit gegenüber dem TNFi Adalimumab aufzeigen konnte.2,3 Zu diesem Ergebnis kam die SPIRIT-H2H-Studie, die die Wirksamkeit und Sicherheit der beiden Medikamente im Direktvergleich untersucht hat.2,3
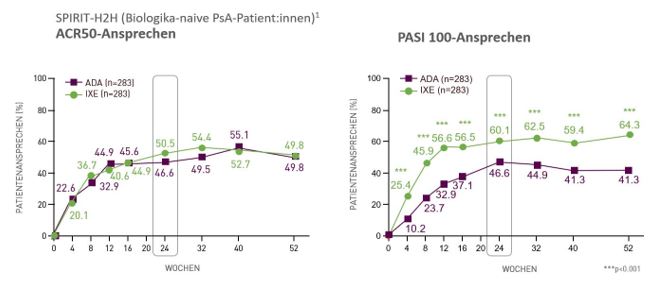
Im direkten Vergleich mit Adalimumab erzielte Taltz® bezogen auf die Gelenksymptome (ACR50-Ansprechen) die gleiche gute Wirksamkeit, war dem TNFα-Inhibitor aber im Hinblick auf die kutane Wirksamkeit (PASI 100-Ansprechen) signifikant (p < 0,001) überlegen (siehe Abb. 1).3
Abbildung 1: ACR50- und PASI 100-Ansprechen bis Woche 52 unter Taltz® oder Adalimumab. ADA, Adalimumab; H2H, Head-to-Head; IXE, Ixekizumab; Modifiziert nach 3.
Taltz® kann demnach einen entscheidenden Bonus für Patient:innen bieten, die unter Gelenk- und Hautbeschwerden leiden.
Bleibt die Wirksamkeit auch langfristig erhalten?
Da die PsA in der Regel ein lebenslanger Begleiter ist, ist es zudem wichtig, Wirksamkeit und Verträglichkeit der Therapeutika über längere Zeit zu betrachten. Einige Biologika verlieren während der Langzeitbehandlung ihre anfänglich gute Wirksamkeit. Für TNFα-Inhibitoren wurde dies in mehreren Studien gezeigt.5-7 So ermittelte das norwegische Register NOR-DMARD, dass unter TNFα-Behandlung 22,7 % der PsA-Patient:innen bereits nach dem ersten Jahr ihre Therapie abbrachen.5
Taltz® zeigte im SPIRIT-Studienprogramm – neben dem signifikanten Ansprechen bereits in Woche 2 – kontinuierlich hohe Ansprechraten bezogen auf die Gelenke und die Haut über den Beobachtungszeitraum von 3 Jahren.8,9
Gutes Ansprechen auf Gelenk- und Hautsymptome: Kombi entscheidend für eine MDA
Neben der Remission wird bei PsA auch eine minimale Krankheitsaktivität (MDA) als Therapieziel empfohlen.10 Diese gilt als erreicht, wenn 5 der folgenden 7 MDA-Kriterien erfüllt sind.10
MDA-Kriterien
- Anzahl schmerzempfindlicher Gelenke ≤ 1
- Anzahl geschwollener Gelenke ≤ 1
- PASI ≤ 1 oder betroffene Fläche der Haut ≤ 3 %
- Schmerzempfinden der Patient:innen: VAS-Score ≤ 15
- Allgemeines Krankheitsempfinden der Patient:innen: VAS ≤ 20
- HAQDI ≤ 0,5
- Anzahl schmerzempfindlicher enthesialer Punkte ≤ 1
Um dieses Ziel zu erreichen ist ein gleichzeitiges, hohes Ansprechen auf Gelenk- und Hautsymptome äußerst wichtig. Die SPIRIT-H2H-Studie hat auch untersucht, wie viele Patient:innen nach 24 Wochen eine MDA erreichten: Im Taltz®-Arm war dieser Anteil signifikant höher als in der Adalimumab-Gruppe (48 % vs. 35 %, p = 0,003). Dies galt auch, wenn die Betroffenen nur unter leichter Psoriasis litten, wie eine Post-Hoc-Analyse zur Studie zeigte: Hier erreichten 46 % der mit Taltz® behandelten und 35 % der mit Adalimumab behandelten Patient:innen eine MDA (p ≤ 0,05).11
Fazit
Taltz® zeigte im direkten Vergleich mit Adalimumab in der PsA-Behandlung eine signifikant bessere Wirksamkeit beim gleichzeitigen Ansprechen auf Haut und Gelenke und beim Erreichen einer MDA.11 Die Wirksamkeit blieb langfristig über einen Zeitraum von 3 Jahren erhalten.8,9
Abkürzungen
Fußnoten
+ Taltz®, allein oder in Kombination mit Methotrexat, ist angezeigt für die Behandlung erwachsener Patienten mit aktiver Psoriasis-Arthritis, die unzureichend auf eine oder mehrere krankheitsmodifizierende Antirheumatika (DMARD) angesprochen oder diese nicht vertragen haben.
Quellen
- Aktuelle Taltz® Fachinformationen
- Mease PJ, et al. Ann Rheum Dis. 2020;79:123-131.
- Smolen JS, et al. Ann Rheum Dis 2020;79:1310-319.
- Coates LC, et al. Nat Rev Rheumatol 2022;18:465-479.
- Heiberg MS, et al. Arthritis Rheum. 2008;59(2):234-240.
- Bekele DI, et al. Rheumatol Int 2022;42(11):1925-1937.
- Deodhar A, Yu D, Semin Arthritis Rheum 2017;27(3):343-350.
- Chandran V, et al. Rheumatology. 2020;59:2774-2784.
- Orbai AM, et al. Rheumatol Ther. 2021;8:199-217.
- Gossec L, et al J Rheumatol. 2018;45(1):6-13.
- Kristensen LE, et al. Rheumatol Ther. 2022;9:109-125.
PP-IX-DE-4156